Modularna asimetrična totalna sinteza biološko aktivnih naravnih produktov z več kiralnimi centri (Z1-2635, 1.9.2020-31.8.2022)
Vodja projekta: doc. dr. Andrej Emanuel Cotman
Povezava do projekta
Radiofarmaki z antagonističnim delovanjem na CCK2R (J1-2483, 1.9.2020-31.8.2023)
Vodja projekta: prof. dr. Marko Anderluh
Povezava do projekta
Odkrivanje in mehanizem delovanja novih spojin vodnic hEag1 kalijevih kanalov s protirakavim delovanjem (N1-0098, 1.1.2019-31.12.2022)
Vodja projekta: prof. dr. Lucija Peterlin Mašič
Povezava do projekta
Razvoj novih zaviralcev Hsp90 s protitumornim delovanjem (J1-1717, 1.7.2019-30.6.2022)
Vodja projekta: izr. prof. dr. Tihomir Tomašič
Povezava do projekta
Pretekli projekti:
Razvoj novih karbamatnih sond za holinesteraze (NC-0009, 1.4.2020-31.3.2021)
Vodja projekta: prof. dr. Stanislav Gobec
Povezava do projekta
Kovalentni zaviralci: zaviranje monoamin oksidaze preko nekatalitskih aminokislinskih ostankov (Z1-1859, 30.6.2019-1.7.2021)
Vodja projekta: doc. dr. Damijan Knez
Povezava do projekta
Identifikacija nepetidnih inhibitorjev imunoproteasoma z metodami razvoja učinkovin na osnovi fragmentov (N1-0068, 1.11.2017-31.10.2020)
Vodja projekta: prof. dr. Stanislav Gobec
Povezava do projekta
Zaviralci butirilholin-esteraze za lajšanje simptomov Alzheimerjeve bolezni (Z1-9195, 1.7.2018-30.6.2021)
Vodja projekta: prof. dr. Stanislav Gobec
Povezava do projekta
Nove protitumorne učinovine napetostno odvisnih kalijevih kanalov hEag1 in njihova validacija v limfomih (J1-9192, 1.7.2018-30.6.2021)
Vodja projekta: prof. dr. Lucija Peterlin Mašič
Povezava do projekta
Razvoj agonistov receptorja NOD2 ter dualnih NOD2/TLR7 agonističnih konjugatov kot novih adjuvansov za cepiva (J3-9256, 1.7.2018-30.6.2021)
Vodja projekta: izr. prof. dr. Žiga Jakopin
Povezava do projekta
Razvoj multifunkcionalnih učinkovin za zdravljenje Alzheimerjeve bolezni (L1-8157, 30.4.2017-30.4.2020)
Vodja projekta: prof. dr. Stanislav Gobec
Povezava do projekta
Boj proti bakterijski rezistenci: optimizacija zaviralcev biosinteze bakterijske stene (L1-6745, 1.7.2014-30.6.2017)
Vodja projekta: prof. dr. Stanislav Gobec
Okužbe z bakterijami, odpornimi na protibakterijske učinkovine, predstavljajo resen izziv za svetovne zdravstvene sisteme. Soočeni smo z naraščanjem odpornosti med gram-pozitivnimi in gram-negativnimi patogeni, ki so povzročitelji bolnišničnih kot tudi izvenbolnišničnih infekcij. Poleg tega predstavljajo, tako imenovane, na antibiotike odporne ‘superbakterije’ resen svetovni zdravstveni problem. V poročilih lahko zasledimo podatek, da vsako leto za posledicami okužbe z na protibakterijske učinkovine odpornimi bakterijami umre 25,000 Evropejcev, pri čemer je ekonomska škoda zaradi tega ocenjena na 1,5 milijarde evrov letno. Po drugi strani pa je kljub nujni potrebi po novih učinkovinah, število novih protibakterijskih učinkovin v razvoju majhno, saj je večina farmacevtske industrije opustila svoje protibakterijske razvojne programe. Naraščajoče število na protibakterijske učinkovine odpornih bakterijskih sevov in majhno število novih učinkovin v razvoju pomenita, da je nujno potrebno povečati intenzivnost iskanja novih. Nujno je odkrivanje novih protibakterijskih učinkovin z uporabo inovativnih metod rešetanja ter uporabo racionalnega načrtovanja na osnovi kristalnih struktur proteinov.
Peptidoglikan je ključna in za bakterijsko celično steno specifična makromolekula. Številni encimi udeleženi pri njegovi biosintezi predstavljajo potencialne tarče za razvoj novih protibakterijskih učinkovin. Skupina prof. Gobca se že 15 let ukvarja z razvojem zaviralcev biosinteze peptidoglikana, pri čemer je razvila številne zaviralce, predvsem encimov Mur (MurA do MurF), DdlB in penicilin vezočih proteinov. S tem projektom želimo nadaljevati dosedanje delo na področju razvoja inhibitorjev biosinteze peptidoglikana, predvsem z izboljšavo inhibitorne aktivnosti in fizikalno-kemijskih ter farmakokinetičnih lastnosti novih spojin.
Izboljšavo zaviralcev biosinteze peptidoglikana bomo dosegli s kombinacijo poglobljenega poznavanja tarčnih encimov, tako lastnega kot tudi znanja mednarodnih partnerjev, in z uporabo najsodobnejših tehnik načrtovanja novih učinkovin. Za projekt bodo koristne tudi natančne strukturne analize, ki nam bodo omogočile hitro in-silico načrtovanje izboljšanih strukturnih ogrodij zaviralcev in kasnejše odkrivanje novih, bolj učinkovitih zaviralcev s protibakterijskim delovanjem. Optimizacija zaviralcev bo temeljila na principu iterativnih ciklov računalniškega načrtovanja, sinteze knjižnic spojin in biokemijskega, strukturnega, mikrobiološkega, predhodnega farmakokinetičnega in toksikološkega vrednotenja. Pričakujemo, da bomo razvili vsaj dve optimizirani spojini vodnici ali klinična kandidata, ki bosta primerni za nadaljnji razvoj v sodelovanju s farmacevtskim podjetjem, ali kot osnova za ustanovitev Start-up podjetja.
Izbrane objave:
1. Hrast Martina, Rožman Kaja, Jukič Marko, Patin Delphine, Gobec Stanislav, Sova Matej. Synthesis and structure-activity relationship study of novel quinazolinone-based inhibitors of MurA. Bioorganic & Medicinal Chemistry Letters, doi: 10.1016/j.bmcl.2017.05.064.
2. Rožman Kaja, Lešnik Samo, Brus Boris, Hrast Martina, Sova Matej, Patin Delphine, Barreteau Hélène, Konc Janez, Janežič Dušanka, Gobec Stanislav. Discovery of new MurA inhibitors using induced-fit simulation and docking. Bioorganic & Medicinal Chemistry Letters 2017, 27, 944-949; doi: 10.1016/j.bmcl.2016.12.082.
3. Šink Roman, Kotnik Miha, Zega Anamarija, Barreteau Hélène, Gobec Stanislav, Blanot Didier, Dessen Andréa, Contreras-Martel Carlos. Crystallographic study of peptidoglycan biosynthesis enzyme MurD: domain movement revisited. PloS One 2016,11, 3, doi: 10.1371/journal.pone.0152075.
4. Sosič Izidor, Anderluh Marko, Sova Matej, Gobec Martina, Mlinarič-Raščan Irena, Derouaux Adeline, Amoroso Ana, Terrak Mohammed, Breukink Eefjan, Gobec Stanislav. Structure-activity relationships of novel tryptamine-based inhibitors of bacterial transglycosylase. Journal of Medicinal Chemistry 2015, 58, 9712-9721, doi: 10.1021/acs.jmedchem.5b01482.
5. Hrast Martina, Sosič Izidor, Šink Roman, Gobec Stanislav. Inhibitors of the peptidoglycan biosynthesis enzymes MurA-F. Bioorganic chemistry 2014, 55, 2-15, doi: 10.1016/j.bioorg.2014.03.008.
Teoretični in praktični vidiki terminologije in terminografije v povezavi s spletnimi terminološkimi viri (L6-4045)
Raziskovalni projekt obsega teoretično in aplikativno delo: raziskovanje in razvijanje terminološke in terminografske teorije (terminološke definicije, posamezne besedne vrste v določeni terminologiji, npr. glagol v pravni terminologiji, antonimija, raziskovanje vpliva angleščine na slovenščino s posebnim poudarkom na terminologiji, slovenjenje terminologije), objava rezultatov v monografijah, člankih, predavanjih, izdelava novih in dodelava že uporabljanih računalniških orodij za obdelavo terminologije (SlovarRed 2.1), oblikovanje in objava specializiranih korpusov, obdelava, prevajanje, normiranje terminologij različnih področij, izdelava in objava normativnih, razlagalnih eno- in večjezičnih slovarjev v knjižni in elektronski obliki (splet), organizacija domačih in mednarodnih strokovnih srečanj, terminološko svetovanje. V okviru projekta se predvideva sodelovanje z zamejskimi Slovenci in pomembnimi evropskimi terminološkimi centri.
Predklinični razvoj novih protimikrobnih učinkovin (L1-4039)
Trajanje projekta: 1.7.2011 – 30.6.2014
Vodja projekta: prof. dr. Stanislav Gobec
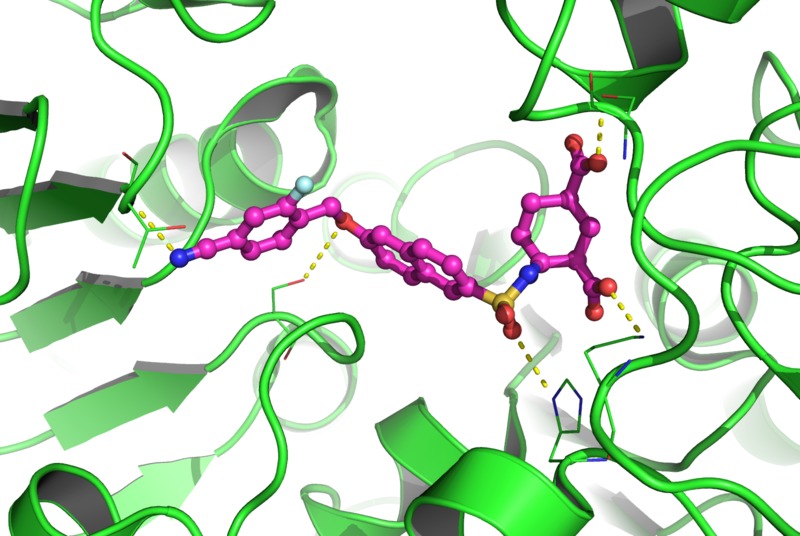
V zadnjih letih zdravstveni sistem postaja vedno bolj odvisen od uporabe antibiotikov. Po drugi strani pa zaradi selekcijskih pritiskov opažamo vedno pogosteje pojavljanje rezistentnih bakterij, ki so že postale globalni zdravstveni problem. Zdravstveni sistemi nujno potrebujejo nova protibakterijska zdravila, ki bi zdravnikom omogočila nove in bolj uspešne načine zdravljenja. S tem projektom želimo prispevati k razvoju novih encimskih inhibitorjev, ki bodo delovali na sintezo bakterijskega peptidoglikana. Ti bodo povzročili smrt bakterij ali pa bakterije naredili bolj občutljive na obstoječe antibiotike. Peptidoglikan je makromolekula, ki je nujno potrebna in specifična za bakterijsko celično steno. Številni encimi, ki so vpleteni v biosintezo peptidoglikana, predstavljajo potencialna tarčna mesta za iskanje novih protibakterijskih učinkovin. Da bi odkrili nove spojine vodnice za razvoj protibakterijskih učinkovin, bomo ciljali na izbrane encime iz različnih bakterijskih vrst, ki katalizirajo znotrajcelične stopnje (Mur ligaze MurC-F in DdlB) in zunajcelične stopnje (penicilin vezoči proteini, PBP) biosinteze peptidoglikana. Strategija odkrivanja inhibitorjev bo temeljila na dostopnih kristalnih strukturah in na kristalnih strukturah, pridobljenih med izvajanjem prijavljenega projekta in bo vključevala de novo načrtovanje molekul, virtualno rešetanje visoke zmogljivosti, kemijsko sintezo knjižnic potencialnih inhibitorjev in njihovo biokemično (ugotavljanje encimske inhibicije), strukturno (rentgenska kristalografija) in mikrobiološko (MIC vrednosti) vrednotenje. Pričakujemo, da bomo razvili več nekovalentnih inhibitorjev kot spojin vodnic iz različnih kemijskih razredov, ki bodo aktivni v nizkem mikromolarnem ali nanomolarnem koncentracijskem območju in bodo imeli protibakterijsko delovanje, kar bo ključen korak pri iskanju novih protibakterijskih učinkovin. Pridobili bomo tudi več kompleksov inhibitor-tarčni encim.
Spojine vodnice, odkrite med izvajanjem predlaganega projekta, bodo predstavljale pomemben korak k razvoju novih protibakterijskih učinkovin in s tem k boju proti naraščajoči rezistenci na antibiotike. Vključenost industrijskega partnerja (Lek d.d.) omogoča prenos rezultatov projekta v slovensko farmacevtsko industrijo.
Izbrane objave:
1. Sosič Izidor, Anderluh Marko, Sova Matej, Gobec Martina, Mlinarič-Raščan Irena, Derouaux Adeline, Amoroso Ana, Terrak Mohammed, Breukink Eefjan, Gobec Stanislav. Structure-activity relationships of novel tryptamine-based inhibitors of bacterial transglycosylase. Journal of medicinal chemistry 2015, 58, 9712-9721, doi: 10.1021/acs.jmedchem.5b01482.
2. Perdih Andrej, Hrast Martina, Barreteau Hélène, Gobec Stanislav, Wolber Gerhard, Šolmajer Tomaž. Inhibitor design strategy based on an enzyme structural flexibility: a case of bacterial MurD ligase. Journal of chemical information and modeling 2014, 54, 1451-1466. doi: 10.1021/ci500104m.
3. Hrast Martina, Anderluh Marko, Knez Damijan, Randall Christopher P., Barreteau Hélène, O'neill Alex J., Blanot Didier, Gobec Stanislav. Design, synthesis and evaluation of second generation MurF inhibitors based ona cyanothiophene scaffold. European Journal of Medicinal Chemistry 2014, 73, 83-96. doi: 10.1016/j.ejmech.2013.11.031.
4. Hrast Martina, Turk Samo, Sosič Izidor, Knez Damijan, Randall Christopher P., Barreteau Hélène, Contreras-Martel Carlos, Dessen Andréa, O'Neill Alex J., Mengin-Lecreulx Dominique, Blanot Didier, Gobec Stanislav. Structure-activity relationships of new cyanothiophene inhibitors of the essential peptidoglycan biosynthesis enzyme MurF. European Journal of Medicinal Chemistry 2013, 66, 32-45. doi: 10.1016/j.ejmech.2013.05.013.
5. Hrast Martina, Vehar Blaž, Turk Samo, Konc Janez, Gobec Stanislav, Janežič Dušanka. Function of the D-Alanine:D-Alanine ligase lid loop : a molecular modeling and bioactivity study. Journal of medicinal chemistry 2012, 55, 6849-6856. doi: 10.1021/jm3006965.
EU projekti
Tekoči EU projekti:
PhD4GlycoDrug (H2020-MSCA-ITN-2017-EJD-765581)
Trajanje projekta: 1.10.2017 – 30.9.2021
Koordinator projekta: prof. dr. Marko Anderluh
PhD4GlycoDrug projekt je skupni evropski doktorski program na področju odkrivanja in razvoja spojin vodnic na osnovi ogljikovih hidratov z delovanjem na lektinske receptorje in encime, ki vežejo in procesirajo ogljikove hidrate. Skupni izobraževalni in raziskovalni program konzorcija PhD4GlycoDrug vključuje vse faze razvoja do spojine vodnice, od identifikacije in karakterizacije novih tarč, odkrivanja novih bioaktivnih spojin, njihove optimizacije in biokemijskega vrednotenja v in vitro in in vivo sistemih.
Pri projektu poleg Fakultete za farmacijo Univerze v Ljubljani kot koordinatorice sodelujejo tudi raziskovalci iz Univerze v Milanu (Italija), Univerze v Utrechtu (Nizozemska), Univerze v Baslu (Švica), Univerze v Lundu (Švedska) in Univerze v Grenoblu (Francija). Projektu je poleg tega priključenih še 6 partnerskih organizacij, in sicer Pamgene International BV (Nizozemska), Centre national de la recherche scientifique (Francija), Acies Bio d.o.o. (Slovenija), SARomics Biostructures AB (Švedska), Red Glead Discovery AB (Švedska) in Elicityl SA (Francija).
Cilj projekta je zaposlitev in izobraževanje 12 mladih raziskovalcev (ESR - early-stage researcher) za obdobje 3 let, ki bodo preko izobraževanja in raziskav pridobili širok nabor znanj na področju odkrivanja potencialnih novih učinkovin na osnovi ogljikovih hidratov. Raziskovalci bodo dve leti delali na matični univerzi in eno leto na eni od partnerskih univerz. Več o projektu najdete na http://cordis.europa.eu/project/rcn/211719_en.html ter na spletni strani projekta: http://www.phd4glycodrug.eu/.
Pretekli EU projekti:
Fakulteta za farmacijo je od 1. novembra 2018 partner na projektu IMI – ENABLE, pri katerem sodelujejo štiri mednarodne farmacevtske družbe (AstraZeneca, Basilea, Evotec in GlaxoSmithKline) ter 24 univerz, raziskovalnih inštitucij, javnih ustanov in 15 majhnih in srednje velikih podjetij. Projekt spada v okvir IMI programa New Drugs for Bad Bugs (ND4BB). Namen projekta ENABLE je predklinični in zgodnji klinični razvoj novih potencialnih učinkovin z delovanjem proti Gram – negativnim bakterijam, ki zaradi pogoste resistence na obstoječe protibakterijske učinkovine predstavljajo velik terapevtski problem in izziv. Cilj projekta, ki je bil v decembru 2019 podaljšan do 31. januarja 2021, je razviti tri spojine vodnice in dva klinična kandidata ter najmanj z eno spojino začeti prvo fazo kliničnih testiranj. Raziskovalna skupina Katedre za farmacevtsko kemijo UL FFA pod vodstvom prof. dr. Danijela Kiklja, v kateri sodelujejo tudi izr. prof. dr. Janez Ilaš, prof.dr. Lucija Peterlin Mašič, izr. prof. dr. Tihomir Tomašič, izr. prof. dr. Anamarija Zega in doc. dr. Nace Zidar, v okviru ENABLE projekta raziskuje optimizacijo v skupini nedavno odkritih in s PCT patentno prijavo zaščitenih ATP-kompetitivnih zaviralcev DNA giraze in topoizomeraze IV z močnim delovanjem proti bakterijam Acinetobacter baumannii in Pseudomonas aeruginosa do spojine vodnice. Projekt ENABLE je na UL FFA omogočil zaposlitev štirih raziskovalcev (dr. Andrej Emanuel Cotman, dr. Davide Benedetto Tiz / dr. Štefan Možina, Federica Fulgheri, mag. farm in Daniela Secci, mag. farm, vanj pa so vključeni tudi mladi raziskovalci Martina Durcik, mag. farm, Žiga Skok, mag. farm. in Maša Sterle, mag. farm. Poleg omenjenih na Vrije Universiteit Amsterdam na raziskovalnem programu UL FFA v okviru projekta dela tudi dr. Guido Janssen. Odbor za upravljanje portfelja vsake tri mesece ocenjuje dosežen napredek in odloča o nadaljnjem financiranju partnerjev projekta ENABLE.
ORCHID
Trajanje projekta: 1.1.2011 – 31.12.2014
Vodja projekta v Sloveniji: prof. dr. Stanislav Gobec
ORCHID je ambiciozen štiriletni projekt, ki ima za cilj razvoj novih potencialnih učinkovin za zdravljenje na več zdravil odporne tuberkuloze (TB). Projekt združuje ekspertizo akademskih inštitucij, vladnih raziskovalnih centrov, neprofitnih organizacij in manjših biotehnoloških podjetij s sredstvi iz 7 okvirnega programa za razvoj EU. Pod vodstvom farmacevtskega podjetja GlaxoSmithKline (GSK) bo več kot 25 znanstvenikov iz vsega sveta združilo svoje moči in znanje v raziskovanju treh področij, ki izkazujejo znaten potencial na področju boja proti na več zdravil odporni tuberkulozi.
Cilj projekta je razviti in validirati novo spojino vodnico, ki bo primerna za testiranje na človeku. Samo sodelovanje tako raznolikih skupin strokovnjakov pa lahko omogoči usklajen napredek vseh treh področij.
Tri glavna raziskovalna področja so:
β-laktami: Novejše raziskave nakazujejo, da bi lahko bili ti širokospektralni antibiotiki učinkoviti tudi za zdravljenje TB. Namen raziskav je razviti nove živalske modele, s katerimi bi bilo mogoče dokazati potencial β-laktamskih antibiotikov za zdravljenje TB.
Novi inhibitorji InhA: GSK je v sodelovanju z TB Alliance pred kratkim odkril serijo spojin, ki lahko inhibirajo znan tarčni encim v TB (InhA), ki je nujen za bakterijsko preživatje. Izbrane spojine iz te serije so bile v laboratojiski pogojih aktivne proti na več zdravil odporni TB (multi drug resistant TB). Prav tako so izkazovale obetavno aktivnost na živalskih modelih Mycobacterium tuberculosis.
Spojine z neznanim mehanizmom delovanja: Sem sodijo spojine, ki so bile odkrite s testi za visoko zmogljivo rešetanje (HTS – high throug put screening) in katerih način delovanja ni znan. Cilj projekta je raziskati njihovo aktivnost.
Izbrane objave:
1. Rožman Kaja, Sosič Izidor, Fernandez-Menendez Raquel, Young Robert J., Mendoza-Losana Alfonso, Gobec Stanislav, Encinas Lourdes. A new 'golden age' for the antitubercular target InhA. Drug Discovery Today 2016, 1-29, doi: 10.1016/j.drudis.2016.09.009.
2. Pajk Stane, Živec Matej, Šink Roman, Sosič Izidor, Neu Margarete, Chung Chun-Wa, Martínez-Hoyos María, Pérez-Herrán Esther, Álvarez-Gómez Daniel, Álvarez-Ruíz Emilio, Mendoza-Losana Alfonso, Castro-Pichel Julia, Barros David, Ballell-Pages Lluís, Young Robert J., Convery Maire A., Encinas Lourdes, Gobec Stanislav. New direct inhibitors of InhA with antimycobacterial activity based on a tetrahydropyran scaffold. European Journal of Medicinal Chemistry 2016, 112, 252-257, doi: 10.1016/j.ejmech.2016.02.008.
3. Šink Roman, Sosič Izidor, Živec Matej, Fernandez-Menendez Raquel, Turk Samo, Pajk Stane, Alvarez-Gomez Daniel, Lopez-Roman Eva Maria, Gonzalez Cortes Carolina, Rullas-Trincado Joaquin, Angulo-Barturen Iñigo, Barros David, Ballell Pages Lluís, Young Robert J., Encinas Lourdes, Gobec Stanislav. Design, synthesis and evaluation of new thiadiazole- based direct inhibitors of enoyl acyl carrier protein reductase (InhA) for the treatment of tuberculosis. Journal of Medicinal Chemistry 2015, 58, 613-624, doi: 10.1021/jm501029r.