Raziskovalno delo
1) Bakterijski encimi in človeški lektini kot tarče za odkrivanje spojin s protimikrobnim delovanjem
Okužbe z bakterijami, odpornimi proti protibakterijskim učinkovinam, predstavljajo resen izziv za svetovne zdravstvene sisteme. Soočeni smo z naraščanjem odpornosti med gram-pozitivnimi in gram-negativnimi patogeni, ki so povzročitelji bolnišničnih kot tudi izvenbolnišničnih infekcij. Raziskovalci na Katedri za farmacevtsko kemijo se v zadnjih 15 letih intenzivno ukvarjamo z odkrivanjem novih protibakterijskih učinkovin, ki zavirajo delovanje encimov, ki so udeleženi v biosintezi peptidoglikana (ligaze MurA-F, D-Ala-D-Ala ligaza B, aspartat ligaza ter transpeptidazna in transglikozilazna domena penicilin vezočih proteinov), zavirajo delovanje DNA-giraze in topoizomeraze IV, ki modulirata topologijo molekule DNA med podvojevanjem, in zavirajo delovanje reduktaze enoil acil prenašalnega proteina (InhA), ki sodeluje v sintezi maščobnih kislin v Mycobacterium tuberculosis. Ukvarjamo se tudi z razvojem antagonistov lektina FimH, ki je ključni virulentni faktor pri okužbi urinarnega trakta z Escherichia coli.
Encimi udeleženi v biosintezi peptidoglikana
Vodja projekta: prof. dr. Stanislav Gobec
Opis: Peptidoglikan je ključna in za bakterijsko celično steno specifična makromolekula. Številni encimi udeleženi pri njegovi biosintezi predstavljajo potencialne tarče za razvoj novih protibakterijskih učinkovin. V zadnjih 15 letih smo v okviru raziskovalnega programa, raziskovalnega projekta ARRS in EU FP6 projekta EUR-INTAFAR razvili številne pomembne zaviralce biosinteze peptidoglikana, predvsem encimov MurA-F, D-Ala-D-Ala ligaze B, aspartat ligaze ter transpeptidazne in transglikozilazne domene penicilin vezočih proteinov. V teku so raziskave s ciljem izboljšati njihovo zaviralno aktivnost, fizikalno-kemijske in ADMET lastnosti. Optimizacija zaviralcev temelji na principu iterativnih ciklov načrtovanja in sinteze analogov, biokemijskega, strukturnega, mikrobiološkega, farmakokinetičnega in toksikološkega vrednotenja.
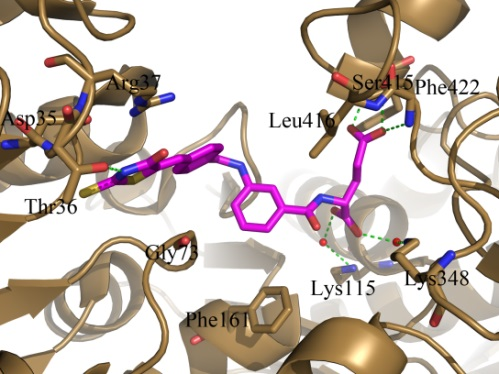
Kristalna struktura ligaze MurD v kompleksu z zaviralcem.
Zadnje objave:
1. Patin Delphine, Turk Samo, Barreteau Hélène, Mainardi Jean-Luc, Arthur Michel, Gobec Stanislav, Mengin-Lecreulx Dominique, Blanot Didier. Unusual substrate specificity of the peptidoglycan MurE ligase from Erysipelothrix rhusiopathiae. Biochimie 2016, 121, 209-218, doi: 10.1016/j.biochi.2015.12.006.
2. Šink Roman, Kotnik Miha, Zega Anamarija, Barreteau Hélène, Gobec Stanislav, Blanot Didier, Dessen Andréa, Contreras-Martel Carlos. Crystallographic study of peptidoglycan biosynthesis enzyme MurD: domain movement revisited. PloS One 2016,11, 3, doi: 10.1371/journal.pone.0152075.
3. Sosič Izidor, Anderluh Marko, Sova Matej, Gobec Martina, Mlinarič-Raščan Irena, Derouaux Adeline, Amoroso Ana, Terrak Mohammed, Breukink Eefjan, Gobec Stanislav. Structure-activity relationships of novel tryptamine-based inhibitors of bacterial transglycosylase. Journal of Medicinal Chemistry 2015, 58, 9712-9721, doi: 10.1021/acs.jmedchem.5b01482.
4.Hrast Martina, Sosič Izidor, Šink Roman, Gobec Stanislav. Inhibitors of the peptidoglycan biosynthesis enzymes MurA-F. Bioorganic chemistry 2014, 55, 2-15, doi: 10.1016/j.bioorg.2014.03.008.
5. Hrast Martina, Anderluh Marko, Knez Damijan, Randall Christopher P., Barreteau Hélène, O'Neill Alex J., Blanot Didier, Gobec Stanislav. Design, synthesis and evaluation of second generation MurF inhibitors based ona cyanothiophene scaffold. European Journal of Medicinal Chemistry 2014, 73, 83-96, doi: 10.1016/j.ejmech.2013.11.031.
DNA-giraza in topoizomeraza IV
Vodja projekta: prof. dr. Danijel Kikelj
Opis: DNA-giraza in topoizomeraza IV sta kot ključna od ATP odvisna encima, ki sodelujeta pri podvajanju DNA, zanimivi tarči za odkrivanje novih protibakterijskih učinkovin. Strukturna podobnost obeh encimov omogoča razvoj dualnih zaviralcev, kar podaljša čas do pojava rezistence. Na osnovi pred kratkim odkritih zaviralcev DNA-giraze iz bakterije Escherichia coli, ki se vežejo v vezavno mesto za ATP, se ukvarjamo z načrtovanjem, sintezo in vrednotenjem novih zaviralcev z optimizirano jakostjo in ADMET lastnostmi s poudarkom na uravnoteženem zaviranju GyrB/ParE za doseganje širokospektralne protibakterijske aktivnosti in zmanjšanja pojava rezistence.
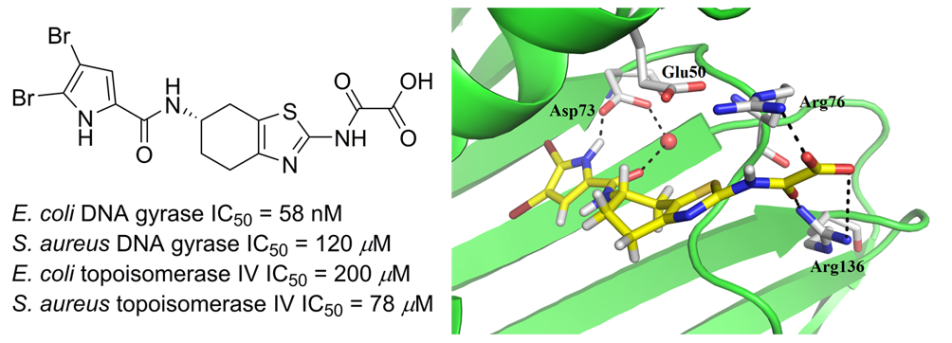
Novi 4,5,6,7-tetrahidrobenzo[1, 2-d]tiazolni zaviralec DNA-giraze.
Zadnje objave:
1. Durcik, Martina, Nyerges, Ákos, Skok, Žiga, Gramec, Darja, Trontelj, Jurij, Zidar, Nace, Ilaš, Janez, Zega, Anamarija, Kikelj, Danijel, Peterlin-Mašič, Lucija, Tomašič, Tihomir, et al. New dual ATP-competitive inhibitors of bacterial DNA gyrase and topoisomerase IV active against ESKAPE pathogens. European Journal of Medicinal Chemistry 2021, 213, 113200 doi: 10.1016/j.ejmech.2021.113200.
2. Tomašič, Tihomir, Zubriené, Asta, Skok, Žiga, Martini, Riccardo, Pajk, Stane, Sosič, Izidor, Ilaš, Janez, Matulis, Daumantas, Bryant, Sharon D. Selective DNA gyrase inhibitors : multi-target in silico profiling with 3D-pharmacophores. Pharmaceuticals 2021, 14, 1-24.
3. Durcik, Martina, Skok, Žiga, Ilaš, Janez, Zidar, Nace, Zega, Anamarija, Szili, Petra, Draskovits, Gábor, Revesz, T., Kikelj, Danijel, Nyerges, Ákos, Pál, Csaba, Peterlin-Mašič, Lucija, Tomašič, Tihomir. Hybrid inhibitors of DNA gyrase A and B : design, synthesis and evaluation. Pharmaceutics 2021, 13, 1-17, doi: 10.3390/pharmaceutics13010006.
4. Skok, Žiga, Barančokova, Michaela, Benek, Ondřej, Durante Cruz, Cristina, Tammela, Päivi, Tomašič, Tihomir, Zidar, Nace, Peterlin-Mašič, Lucija, Zega, Anamarija, Kikelj, Danijel, Ilaš, Janez, et al. Exploring the chemical space of benzothiazole-based DNA gyrase B inhibitors. ACS Medicinal Chemistry Letters 2020, 11, 2433-2440, doi: 10.1021/acsmedchemlett.0c00416.
5. Nyerges, Ákos, Tomašič, Tihomir, Durcik, Martina, Revesz, T., Szili, Petra, Skok, Žiga, Zidar, Nace, Ilaš, Janez, Zega, Anamarija, Kikelj, Danijel, Peterlin-Mašič, Lucija, et al. Rational design of balanced dual-targeting antibiotics with limited resistance. PLoS Biology 2020, 18, 1-31, 10.1371/journal.pbio.3000819.
InhA
Vodja projekta: prof. dr. Stanislav Gobec
Opis: Kot nadaljevanje dela, opravljenega v okviru EU FP7 projekta ORCHID (koordinator GlaxoSmithKline), razvijamo nove zaviralce reduktaze enoil acil prenašalnega proteina (InhA), ki sodeluje v sintezi maščobnih kislin v Mycobacterium tuberculosis. Strategija odkrivanja novih zaviralcev temelji na dostopnih kristalnih strukturah InhA in vključuje de-novo načrtovanje, virtualno rešetanje, kemijsko sintezo inhibitorjev in biokemično, strukturno, mikrobiološko in toksikološko vrednotenje.
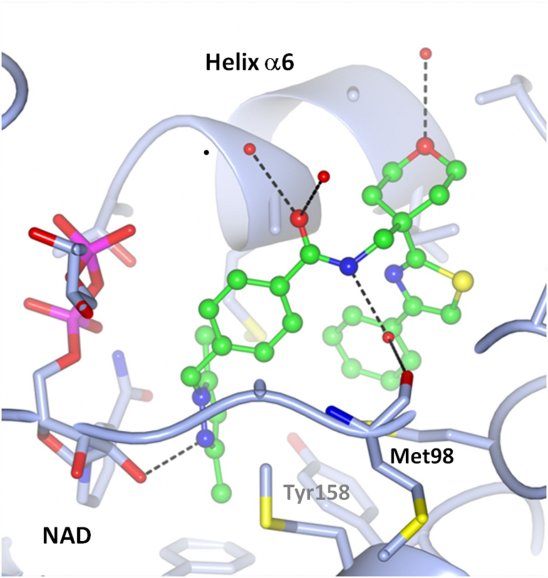
Kristalna struktura zaviralca s tetrahidropiranskim skeletom v aktivnem mestu InhA
Zadnje objave:
1. Štular Tanja, Lešnik Samo, Rožman Kaja, Schink Julia, Zdouc Mitja, Ghysels An, Liu Feng, Aldrich Courtney C., Haupt V. Joachim, Salentin Sebastian, Daminelli Simone, Schroeder Michael, Langer Thierry, Gobec Stanislav, Janežič Dušanka, Konc Janez. Discovery of Mycobacterium tuberculosis InhA inhibitors by binding sites comparison and ligands prediction. Journal of medicinal chemistry 2016, 59, 11069-11078.
2. Rožman Kaja, Sosič Izidor, Fernandez-Menendez Raquel, Young Robert J., Mendoza-Losana Alfonso, Gobec Stanislav, Encinas Lourdes. A new 'golden age' for the antitubercular target InhA. Drug Discovery Today 2016, 1-29, doi: 10.1016/j.drudis.2016.09.009.
3. Pajk Stane, Živec Matej, Šink Roman, Sosič Izidor, Neu Margarete, Chung Chun-Wa, Martínez-Hoyos María, Pérez-Herrán Esther, Álvarez-Gómez Daniel, Álvarez-Ruíz Emilio, Mendoza-Losana Alfonso, Castro-Pichel Julia, Barros David, Ballell-Pages Lluís, Young Robert J., Convery Maire A., Encinas Lourdes, Gobec Stanislav. New direct inhibitors of InhA with antimycobacterial activity based on a tetrahydropyran scaffold. European Journal of Medicinal Chemistry 2016, 112, 252-257, doi: 10.1016/j.ejmech.2016.02.008.
4. Šink Roman, Sosič Izidor, Živec Matej, Fernandez-Menendez Raquel, Turk Samo, Pajk Stane, Alvarez-Gomez Daniel, Lopez-Roman Eva Maria, Gonzalez Cortes Carolina, Rullas-Trincado Joaquin, Angulo-Barturen Iñigo, Barros David, Ballell Pages Lluís, Young Robert J., Encinas Lourdes, Gobec Stanislav. Design, synthesis and evaluation of new thiadiazole- based direct inhibitors of enoyl acyl carrier protein reductase (InhA) for the treatment of tuberculosis. Journal of Medicinal Chemistry 2015, 58, 613-624, doi: 10.1021/jm501029r.
FimH
Vodja projekta: prof. dr. Marko Anderluh
Opis: Lektin FimH je ključni virulentni faktor pri okužbi urinarnega trakta z bakterijo Escherichia coli, ki se začne s tvorbo biofilma preko adhezije FimH na epitelij sečnega mehurja. Preprečevanje interakcije med FimH in manoziliranimi proteini z antagonisti FimH je obetaven pristop za preprečevanje okužb urinarnega trakta z E. coli. Nekateri α-D-manozilglikokonjugati delujejo kot inhibitorji adhezije FimH, vendar jim niso dokazali terapevtske uporabnosti, zato je cilj razvoj novih, terapevtsko uporabnih FimH antagonistov kot protibakterijskih zdravilnih učinkovin.
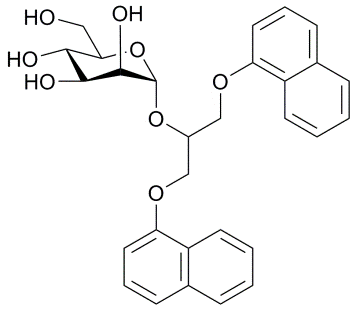
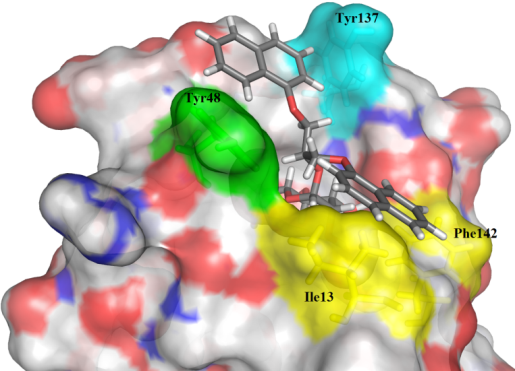
Novi α-D-manopiranozidi kot antagonisti FimH.
Zadnje objave:
1. Tomašič Tihomir, Rabbani Said Rahnamaye, Jakob Roman P., Reisner Andreas, Jakopin Žiga, Maier Timm, Ernst Beat, Anderluh Marko. Does targeting Arg98 of FimH lead to high affinity antagonists?. European Journal of Medicinal Chemistry 2021, 211, 1-16. doi: 10.1016/j.ejmech.2020.113093.
2. Tomašič Tihomir, Rabbani Said Rahnamaye, Gobec Martina, Mlinarič-Raščan Irena, Podlipnik Črtomir, Ernst Beat, Anderluh Marko. Branched α-D-mannopyranosides; a new class of potent FimH antagonists. MedChemComm 2014, 5, 1247-1253, doi: 10.1039/C4MD00093E.
2) Imunoproteasom, NOD in Toll-u podobni receptorji kot tarče za razvoj imunomodulatorjev
Receptorji NOD
Vodja projekta: doc. dr. Žiga Jakopin
Opis: NOD receptorji so znotrajcelični receptorji udeleženi v prepoznavanju patogenov v sklopu prirojenega imunskega sistema. Tarča muramil dipeptida (MDP), najmanjšega imunostimulatornega fragmenta bakterijskega peptidoglikana, je receptor NOD2, na katerega MDP deluje kot agonist. Agonisti NOD so zato potencialne imunostimulatorne in posredno tudi protibakterijske zdravilne učinkovine. Naravna liganda za NOD1 in NOD2 sta dipeptida D-Glu-mezo-DAP in MDP, majhna fragmenta peptidoglikana. Nedavno smo odkrili imunostimulatorne analoge MDP kot agoniste NOD2 in analoge D-Glu-mezo-DAP kot agoniste NOD1. Trenutno potekajo raziskave na področju odkrivanja NOD1 in NOD2 agonistov z uporabo koncepta peptido- in glikomimetikov ter odkrivanje NOD1 in NOD2 antagonistov, ki lahko delujejo protivnetno.
Zadnje objave:
1. Keček Kaja, Urbančič Dunja, Gobec Martina, Pekošak Aleksandra, Tomašič Tihomir, Anderluh Marko, Mlinarič-Raščan Irena, Jakopin Žiga. Identification of indole scaffold-based dual inhibitors of NOD1 and NOD2. Bioorganic & Medicinal Chemistry 2016, 24, 5221-5234, doi: 10.1016/j.bmc.2016.08.044.
2. Gobec Martina, Mlinarič-Raščan Irena, Sollner Dolenc Marija, Jakopin Žiga. Structural requirements of acylated Gly-l-Ala-d-Glu analogs for activation of the innate immune receptor NOD2. European Journal of Medicinal Chemistry 2016, 116, 1-12, doi: 10.1016/j.ejmech.2016.03.030.
3. Jakopin Žiga. Nucleotide-binding oligomerization domain (NOD) inhibitors: a rational approach toward inhibition of NOD signaling pathway. Journal of Medicinal Chemistry 2014, 57, 6897-6918, doi: 10.1021/jm401841p.
4. Jakopin Žiga, Gobec Martina, Kodela Jaka, Hazdovac Toni, Mlinarič-Raščan Irena, Sollner Dolenc Marija. Synthesis of conformationally constrained [gamma]-D-glutamyl-meso -diaminopimelic acid derivatives as ligands of nucleotide-binding oligomerization domain protein 1 (Nod1). European Journal of Medicinal Chemistry 2013, 69, 232-243. doi: 10.1016/j.ejmech.2013.08.022.
5. Jakopin Žiga, Gobec Martina, Mlinarič-Raščan Irena, Sollner Dolenc Marija. Immunomodulatory properties of novel nucleotide oligomerization domain 2 (Nod2) agonistic desmuramyldipeptides. Journal of Medicinal Chemistry 2012, 55, 6478-6488, doi: 10.1021/jm300503b.
Toll-u podobni receptorji
Vodja projekta: prof. dr. Stanislav Gobec
Opis: Toll-u podobni receptorji (TLR) predstavljajo pomembno komponento človeškega prirojenega imunskega sistema. Prepoznavajo specifične strukturno različne molekularne vzorce, kot so molekularne komponente mikroorganizmov ali endogene molekule, ki izhajajo iz poškodbe tkiv. Do danes je bilo odkritih 13 različnih sesalskih TLR, med katerimi so identificirali 10 funkcionalnih TLR pri človeku. TLR predstavljajo validirane tarče za razvoj učinkovin za zdravljenje raka, bakterijskih in virusnih okužb in sepse, revmatoidnega artritisa in avtoimunih bolezni. V naših raziskavah smo se osredotočili na iskanje modulatorjev, agonistov in/ali antagonistov TLR4, TLR7 in TLR8. Za načrtovanje želenih novih spojin uporabljamo napredne računalniško podprte metode načrtovanja (in silico metode), izhajamo pa iz objavljenih kristalnih struktur receptorjev ali struktur ligandov. Z virtualnim rešetanjem na osnovi strukture receptorja in/ali liganda smo že odkrili prve antagoniste TLR4, trenutno pa poteka načrtovanje, sinteza in vrednotenje novih agonistov TLR7 in TLR8 kot potencialnih imunomodulatornih spojin za zdravljenje rakavih obolenj.
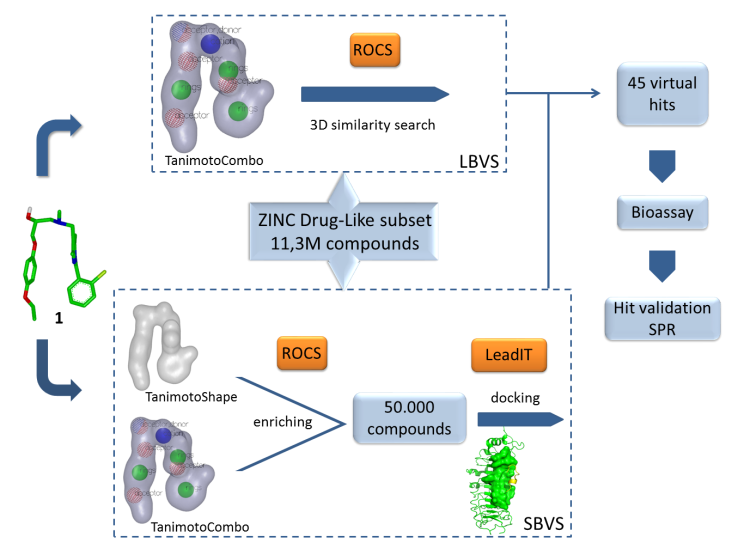
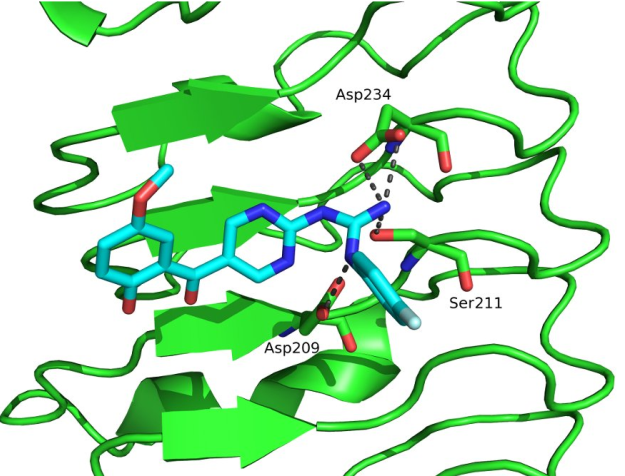
Načrtovanje novih antagonistov TLR4 in predlagana vezava spojine zadetka (modra) v aktivno mesto TLR4 (zelena) na osnovi sidranja.
Zadnje objave:
1. Sova Matej, Rožman Kaja, Švajger Urban, Rožman Primož, Gobec Stanislav. Synthesis and biological evaluation of N-aryl-N'-(5-(2-hydroxybenzoyl)pyrimidin-2-yl)guanidines as toll-like receptor 4 antagonists synthesis of guanidine-based TLR4 antagonists. Medicinal Chemistry 2016, 12, doi: 10.2174/1573406412666160314151900.
2. Švajger Urban, Horvat Žiga, Knez Damijan, Rožman Primož, Turk Samo, Gobec Stanislav. New antagonists of toll-like receptor 7 discovered through 3D ligand-based virtual screening. Medicinal Chemistry Research 2015, 24, 362-371, doi: 10.1007/s00044-014-1127-5.
3. Švajger Urban, Brus Boris, Turk Samo, Sova Matej, Hodnik Vesna, Anderluh Gregor, Gobec Stanislav. Novel toll-like receptor 4 (TLR4) antagonists identified by structure- and ligand-based virtual screening. European Journal of Medicinal Chemistry 2013, 70, 393-399, doi: 10.1016/j.ejmech.2013.10.019.
Imunoproteasom
Vodja projekta: prof. dr. Stanislav Gobec
Opis: Povišano ekspresijo imunoproteasoma pri vretenčarjih povezujejo z avtoimunskimi, nevrodegenerativnimi ter nekaterimi malignimi obolenji. Večina znanih zaviralcev imunoproteasoma je nespecifičnih, saj hkrati zavirajo tudi konstitutivni proteasom. Nedavno opravljena raziskave so nakazale, da bi selektivni zaviralci imunoproteasoma lahko imeli manj neželenih učinkov kot zaviralci, ki hkrati zaviralno delujejo na obe podvrsti encima. Na osnovi znane kristalne strukture imunoproteasoma razvijamo selektivne zaviralce imunoproteasoma. Vse pripravljene spojine najprej vrednotimo na izoliranem encimu, nato pa ovrednotimo njihovo imunomodulatorno delovanje z ustreznimi in vitro funkcijskimi testi.
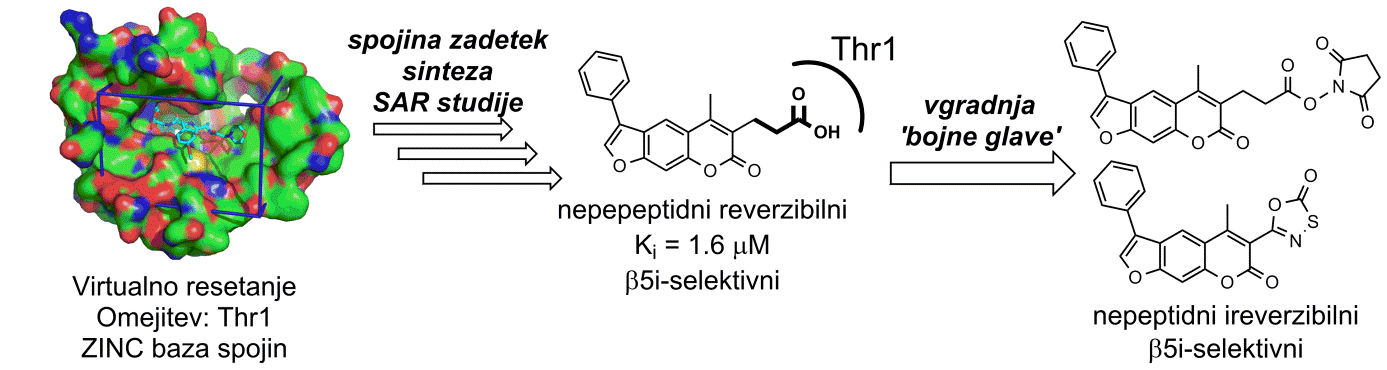
Primer strukturno podprtega odkritja in razvoja selektivnih zaviralcev imunoproteasoma.
Zadnje objave in patenti:
1. Sosič Izidor, Gobec Martina, Brus Boris, Knez Damijan, Živec Matej, Konc Janez, Lešnik Samo, Ogrizek Mitja, Obreza Aleš, Žigon Dušan, Janežič Dušanka, Mlinarič-Raščan Irena, Gobec Stanislav. Nonpeptidic selective inhibitors of the chymotrypsin-like (ß5i) subunit of the immunoproteasome. Angewandte Chemie 2016, 55, 5745-5748, doi: 10.1002/anie.201600190.
2. Sosič Izidor, Gobec Martina, Brus Boris, Knez Damijan, Obreza Aleš, Mlinarič-Raščan Irena, Gobec Stanislav. Derivati psoralena kot nepeptidni zaviralci kimotripsinske aktivnosti imunoproteasoma: 24952 (A), 2016-09-30. Ljubljana: Urad Republike Slovenije za intelektualno lastnino.
3) Ionski kanali, holinesteraze in agregacija amiloida beta kot tarče za zdravljenje nevrodegenerativnih bolezni
Ionski kanali
Vodja projekta: prof. dr. Danijel Kikelj
Opis: Napetostno odvisni natrijevi (Nav) in kalijevi (Kv) kanali so prisotni v številnih vrstah vzdražnih celic, kot so miociti, endokrine celice in nevroni centralnega in perifernega živčnega sistema, kjer so ključni za sprožitev in prevajanje električnih signalov. Motnje v delovanju Nav in Kv kanalov lahko privedejo do pretirane vzdražnosti teh celic, kar se lahko odrazi v različnih nevrodegenerativnih obolenjih, kronični bolečini, epilepsijah in različnih oblikah raka. Kristalne strukture bakterijskih Nav in Kv kanalov so dobro izhodišče za načrtovanje selektivnih modulatorjev Nav in Kv kanalov. Pred kratkim smo zgradili homologni model človeških Nav in pripravili več strukturnih razredov modulatorjev Nav in Kv. Na njihovi osnovi poteka načrtovanje in sinteza novih izboljšanih analogov in njihovo vrednotenje v elektrofizioloških testih na različnih podtipih Nav in Kv.
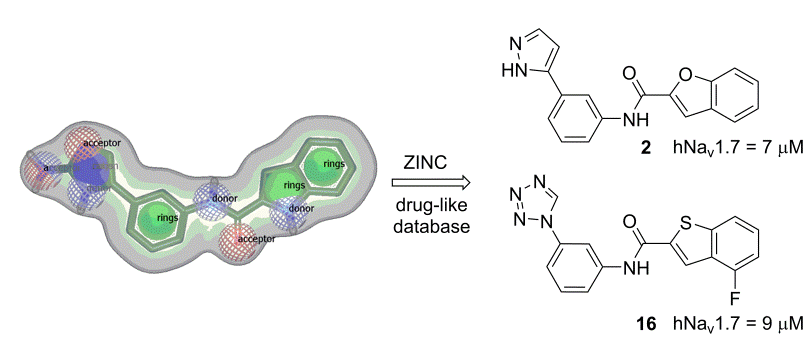
Odkritje novih blokatorjev napetostno odvisnih natrijevih kanalov 1.7 s pomočjo virtualnega rešetanja.
Zadnje objave:
1. Rogers Marc, Zidar Nace, Kikel, Danijel, Kirby Robert W. Characterization of endogenous sodium channels in the ND7-23 neuroblastoma cell line: implications for use as a heterologous ion channel expression system suitable for automated patch clamp screening. Assay and drug development technologies 2016, 14, 109-130, doi: 10.1089/adt.2016.704.
2. Jukič Marko, Frlan Rok, Chan Fiona, Kirby Robert W., Madge David J., Tytgat Jan, Peigneur Steve, Anderluh Marko, Kikelj Danijel. Synthesis and biological evaluation of piperazine derivatives as novel isoform selective voltage-gated sodium (Nav) 1.3 channel modulators. Medicinal Chemistry Research 2015, 24, 2366-2380, doi: 10.1007/s00044-014-1300-x.
3. Zidar Nace, Jakopin Žiga, Madge David J., Chan Fiona, Tytgat Jan, Peigneur Steve, Sollner Dolenc Marija, Tomašič Tihomir, Ilaš Janez, Peterlin Mašič Lucija, Kikelj Danijel. Substituted 4-phenyl-2-aminoimidazoles and 4-phenyl-4,5-dihydro-2-aminoimidazoles as voltage-gated sodium channel modulators. European Journal of Medicinal Chemistry 2014, 74, 23-30, doi: 10.1016/j.ejmech.2013.12.034.
4. Peigneur Steve, Žula Aleš, Zidar Nace, Chan-Porter Fiona, Kirby Robert, Madge David J., Ilaš Janez, Kikelj Danijel, Tytgat Jan. Action of clathrodin and analogues on voltage-gated sodium channels. Marine drugs 2014, 12, 2132-2143, doi: 10.3390/md12042132.
5. Tomašič Tihomir, Hartzoulakis Basil, Zidar Nace, Chan Fiona, Kirby Robert W., Madge David J., Peigneur Steve, Tytgat Jan, Kikelj Danijel. Ligand- and structure-based virtual screening for clathrodin-derived human voltage-gated sodium channel modulators. Journal of Chemical Information and Modeling 2013, 53, 3223-3232, doi: 10.1021/ci400505e.
Holinesteraze in monoamin oksidaze
Vodja projekta: prof. dr. Stanislav Gobec
Opis: Butirilholin esteraza (BChE) predstavlja dobro terapevtsko alternativo za povečanje bolezensko zmanjšanega holinergičnega prenosa in izboljšanje kognitivnih sposobnosti pri Alzheimerjevi bolezni (AB). Za proces nevrodegeneracije pri AB je poleg agregacije in kopičenja amiloida β (Aβ) značilen še povečan oksidativni stres, porušena homeostaza kovinskih ionov, vnetje v centralnem živčnem sistemu in povečana aktivnost monoamin oksidaz A in B (MAO-A in MAO-B). Povečano aktivnost MAO-A so nedavno povezali tudi s patološkimi stanji kot so rak, kardiomiopatija in sladkorna bolezen. V skladu z obujenim zanimanjem za te tarče smo se v okviru naših raziskav osredotočili na razvoj selektivnih zaviralcev BChE, MAO-A in MAO-B ter na odkrivanje multifunkcionalnih spojin, ki hkrati ciljajo vsaj dva navedena encima. Pri načrtovanju multifunkcionalnih ligandov želimo zmanjšati predvsem nevrovnetje ter preprečiti škodljive posledice v kaskadi Aβ.
Tekom raziskav smo razvili dva večja razreda nizko nanomolarnih in pikomolarnih selektivnih zaviralcev BChE. Selektivni zaviralci BChE s piperidinskim skeletom (glej sliko)prehajajo krvno-možgansko pregrado in vivo, izboljšajo spomin, učne sposobnosti in kognitivne funkcije v skopolaminskem mišjem modelu kognitivnega pomanjkanja. Poleg tega smo s študijo na psih s pasjo demenco pokazali, da sulfonamidni zaviralec BChE izboljša kognitivne funkcije psov in njihovo splošno kvaliteto življenja. Na osnovi selektivnih zaviralcev BChE smo razvili tudi več multifunkcionalnih ligandov. V sodelovanju s tujimi partnerji smo razvili 11C PET sledilec, ovrednotili njegovo stabilnost in biodistribucijo in vivo ter izvedli longitudinalno študijo aktivnosti BChE v možganih kontrolnih in 5xFAD živali (model AB) z uporabo pozitronske emisijske tomografije v kombinaciji z računalniško tomografijo. Rezultati študije nedvoumno potrjujejo, da je BChE obetaven biološki označevalec za zgodnjo obliko AB. Derivati triptofana predstavljajo drugo večjo serijo selektivnih zaviralcev BChE. Njihove razrešene kristalne strukture v kompleksu z BChE so omogočile nadaljnjo optimizacijo aktivnosti na tarči ter izboljšanje ADMET lastnosti. In vivo študija varnosti in učinkovitosti spojine vodnice iz serije derivatov triptofana je pokazala, da spojina izboljša spominske funkcije brez neželenih stranskih motoričnih učinkov. Serija 1-propargil-4-stirilpiperidinu podobnih analogov predstavlja edinstven primer stereoselektivne aktivnosti cis/trans izomerov; cis izomeri so močni zaviralci MAO-A, medtem ko trans analogi selektivno zavirajo samo MAO-B. Dokazani pozitivni in vivo rezultati zaviralcev BChE in MAO predstavljajo odlično odskočno desko za nadaljnji razvoj novih in varnih zdravil za terapijo nevrodegenerativnih obolenj.

Zadnje objave:
1. Maja Zakošek Pipan, Sonja Prpar Mihevc, Malan Štrbenc, Urban Košak, Ilija German Ilić, Jurij Trontelj, Simon Žakelj, Stanislav Gobec, Darja Pavlin, Gregor Majdič. Treatment of canine cognitive dysfunction with novel butyrylcholinesterase inhibitor. Scientific Reports. 2021, 11, 18098, doi: 10.7150/thno.54589. doi: 10.1038/s41598-021-97404-2.
2. Luka Rejc, Vanessa Gómez-Vallejo, Ana Joya, Óscar Moreno, Ander Egimendia, Pilar Castellnou, Xabier Ríos-Anglada, Unai Cossío, Urban Košak, Damijan Knez, Stanislav Gobec, Mariel Marder, Abraham Martin, Jordi Llop. Longitudinal evaluation of a novel BChE PET tracer as an early in vivo biomarker in the brain of a mouse model for Alzheimer disease. Theranostics. 2021, 11, 6542–6559, doi: 10.7150/thno.54589.
3. Anže Meden, Damijan Knez, Natalia Malikowska-Racia, Xavier Brazzolotto, Florian Nachon, Jurij Svete, Kinga Sałat, Uroš Grošelj, Stanislav Gobec. Structure-activity relationship study of tryptophan-based butyrylcholinesterase inhibitors. European Journal of Medicinal Chemistry. 2020, 208, 112766, doi: 10.1016/j.ejmech.2020.112766.
4. Urban Košak, Nika Strašek, Damijan Knez, Marko Jukič, Simon Žakelj, Abida Zahirović, Anja Pišlar, Xavier Brazzolotto, Florian Nachon, Janko Kos, Stanislav Gobec. N-Alkylpiperidine carbamates as potential anti-Alzheimer's agents. European Journal of Medicinal Chemistry. 2020, 197, 112282, doi: 10.1016/j.ejmech.2020.112282.
5. Damijan Knez, Natalia Colettis, Luca G. Iacovino, Matej Sova, Anja Pišlar, Janez Konc, Samo Lešnik, Josefina Higgs, Fabiola Kamecki, Irene Mangialavori, Ana Dolšak, Simon Žakelj, Jurij Trontelj, Janko Kos, Claudia Binda, Mariel Nora Marder, Stanislav Gobec. Stereoselective activity of 1-propargyl-4-styrylpiperidine-like analogues that can discriminate between monoamine oxidase isoforms A and B. Journal of Medicinal Chemistry 2020, 63, 1361–1387, doi: 10.1021/acs.jmedchem.9b01886.
6. Stane Pajk, Damijan Knez, Urban Košak, Maja Zorović, Xavier Brazzolotto, Nicolas Coquelle, Florian Nachon, Jacques-Philippe Colletier, Marko Živin, Jure Stojan, Stanislav Gobec. Development of potent reversible selective inhibitors of butyrylcholinesterase as fluorescent probes. Journal of Enzyme Inhibition and Medicinal Chemistry 2020, 35, 498–505, doi: 10.1080/14756366.2019.1710502.
7. Anže Meden, Damijan Knez, Marko Jukič, Xavier Brazzolotto, Marija Gršič, Anja Pišlar, Abida Zahirović, Janko Kos, Florian Nachon, Jurij Svete, Stanislav Gobec, Uroš Grošelj. Tryptophan-derived butyrylcholinesterase inhibitors as promising leads against Alzheimer's disease. Chemical Communications 2019, 55, 3765–3768, doi: 10.1039/C9CC01330J.
8. Urban Košak, Boris Brus, Damijan Knez, Simon Žakelj, Jurij Trontelj, Anja Pišlar, Roman Šink, Marko Jukič, Marko Živin, Adrian Podkowa, Florian Nachon, Xavier Brazzolotto, Jure Stojan, Janko Kos, Nicolas Coquelle, Kinga Sałat, Jacques-Philippe Colletier, Stanislav Gobec. The magic of crystal structure-based inhibitor optimization: development of a butyrylcholinesterase inhibitor with picomolar affinity and in vivo activity. Journal of Medicinal Chemistry 2018, 61, 119–139, doi: 10.1021/acs.jmedchem.7b01086..
4) Katepsin B, pregnanski-X receptor in indolamin 2,3-dioksigenaza kot tarče za odkrivanje protitumornih učinkovin
Katepsin B
Vodja projekta: prof. dr. Stanislav Gobec
Opis: KatB sodeluje v procesih, ki prispevajo k napredovanju raka. Pred kratkim smo odkrili 5-nitro-8-hidroksikinolin kot nekovalentni, reverzibilni in selektivni zaviralec KatB. Pripravili smo tudi optimizirane zaviralce KatB, načrtovane na osnovi naše kristalne strukture kompleksa KatB-zaviralec, ki so zmanjšali tumorsko progresijo preko zaviranja KatB. Na osnovi strukturnih informacij poteka načrtovanje in sinteza nove generacije zaviralcev KatB z izboljšanimi lastnostmi, ki jih vrednotimo v in vitro funkcijskih testih in v in vivo mišjih modelih.
Vzporedno s temi raziskavami pripravljamo tudi rutenijeve komplekse, pri katerih različni derivati 8-hidroksikinolina nastopajo kot eden izmed ligandov. Tovrstne kovinske komplekse najprej vrednotimo kot zaviralce katepsina B, nato pa jim v in vitro pogojih določimo še zmožnost zaviranja razgradnje zunajceličnega matriksa.
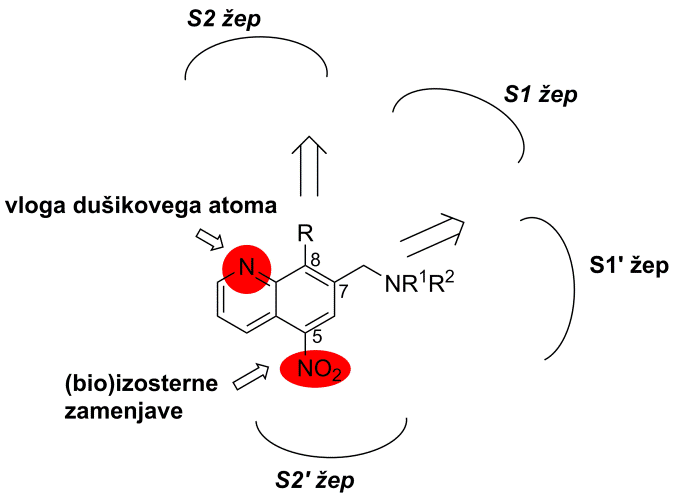
Shematski prikaz strukturnih modifikacij na molekuli nitroksolina.
Zadnje objave:
1. Mitrović Ana, Kljun Jakob, Sosič Izidor, Gobec Stanislav, Turel Iztok, Kos Janko. Clioquinol-ruthenium complex impairs tumour cell invasion by inhibiting cathepsin B activity. Dalton transactions 2016, doi: 10.1039/C6DT02369J.
2. Ogrizek Mitja, Turk Samo, Lešnik Samo, Sosič Izidor, Hodošček Milan, Mirković Bojana, Kos Janko, Janežič Dušanka, Gobec Stanislav, Konc Janez. Molecular dynamics to enhance structure-based virtual screening on cathepsin B. Journal of Computer-Aided Molecular Design 2015, 29, 707-712, doi: 10.1007/s10822-015-9847-2.
3. Mirković Bojana, Markelc Boštjan, Butinar Miha, Mitrović Ana, Sosič Izidor, Gobec Stanislav, Vasiljeva Olga, Turk Boris, Čemažar Maja, Serša Gregor, Kos Janko. Nitroxoline impairs tumor progression in vitro and in vivo by regulating cathepsin B activity. Oncotarget 2015, 6, 19027-19042.
4. Sosič, Izidor, Mirković, Bojana, Arenz, Katharina, Štefane, Bogdan, Kos, Janko, Gobec, Stanislav. Development of new cathepsin B inhibitors: combining bioisosteric replacements and structure-based design to explore the structure-activity relationships of nitroxoline derivatives. Journal of Medicinal Chemistry 2013, 56, 521-533, doi: 10.1021/jm301544x.
5. Mirković Bojana, Renko Miha, Turk Samo, Sosič Izidor, Jevnikar Zala, Obermajer Nataša, Turk Dušan, Gobec Stanislav, Kos Janko. Novel mechanism of cathepsin B inhibition by antibiotic nitroxoline and related compounds. ChemMedChem 2011, 6, 1351-1356, doi: 10.1002/cmdc.201100098.
Pregnanski-X receptor
Vodja projekta: prof. dr. Danijel Kikelj
Opis: Prekomerna ekspresija pregnanskih-X receptorjev (PXR) v številnih rakavih celičnih linijah kaže na pomembnost PXR kot tarče za razvoj protitumornih učinkovin, ki bi lahko zmanjševale rezistenco na protirakavo terapijo. Na osnovi steroidov iz morskih organizmov in preliminarnih rezultatov v okviru EU FP7 projekta MAREX smo s pomočjo steroidomimetičnega pristopa pripravili nove modulatorje PXR, katerih optimizacija je v teku.
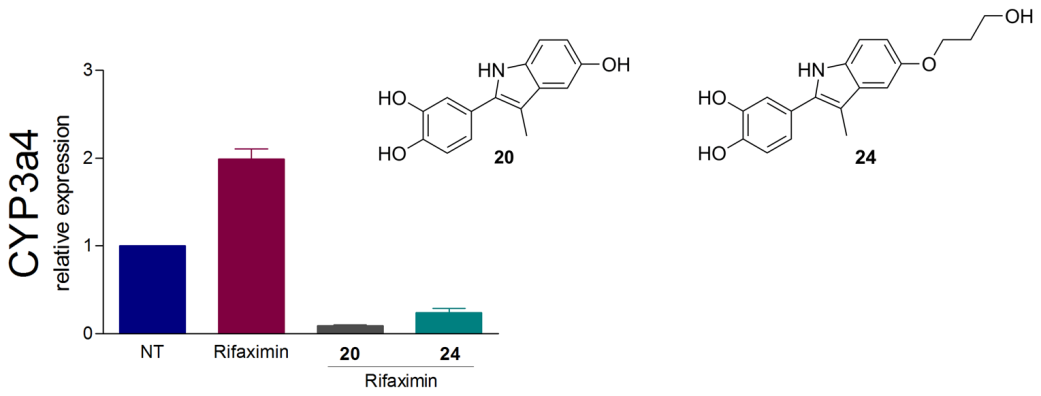
Mimetiki solomonsterolov A in B z bazedoksifenskim skeletom kot novi antagonisti pregnanskega-X receptorja.
Zadnje objave:
1. Hodnik Žiga, Tomašič Tihomir, Smodiš Domen, D'Amore Claudio, Peterlin Mašič Lucija, Fiorucci Stefano, Kikelj Danijel. Diethylstilbestrol-scaffold-based pregnane X receptor modulators. European Journal of Medicinal Chemistry 2015, 103, 551-562, doi: 10.1016/j.ejmech.2015.09.005.
2. Hodnik Žiga, Peterlin Mašič Lucija, Tomašič Tihomir, Smodiš Domen, D'Amore Claudio, Fiorucci Stefano, Kikelj Danijel. Bazedoxifene scaffold-based mimetics of solomonsterols A and B as novel pregnane X receptor antagonists. Journal of Medicinal Chemistry 2014, 57, 4819-4833, doi: 10.1021/jm500351m.
Indolamin 2,3-dioksigenaza
Vodja projekta: doc. dr. Matej Sova
Opis: Encim, ki je vpleten v kinureninsko metabolno pot triptofana, predstavlja zelo interesantno tarčo za imunoterapijo raka. Indolamin 2,3-dioksigenaza 1 (IDO1) je hem-vsebujoči encim, ki katalizira oksidacijo L-triptofana do N-formilkinurenina, ki je začetni in omejujoči korak pri kinureninski metabolni poti. Visoka ekspresija IDO1, ki so jo našli v tumorskih celicah, omogoča izogibanje imunskemu sistemu, kar je povezano s slabo prognozo pri številnih rakavih obolenjih. Zato je dandanes delovanje IDO1 eden izmed pomembnejših faktorjev pri proliferaciji in širjenju raka. S pomočjo strukturno-podprtega načrtovanja bomo poiskali nove inhibitorje IDO-1, s pomočjo celičnih funkcijskih testov pa bomo ovrednotili njihove potencialne protitumorne učinke.

Strukturno-podprto načrtovanje novih zaviralcev encima indolamin 2,3-deoksigenaze.
Zadnje objave:
1. Dolšak Ana, Bratkovič Tomaž, Mlinarič Larisa, Ogorevc Eva, Švajger Urban, Gobec Stanislav, Sova Matej. Novel selective IDO1 inhibitors with isoxazolo[5,4-d]pyrimidin-4(5H)-one scaffold. Pharmaceuticals 2021, 14, 1-18, doi: 10.3390/ph14030265.
5) Sinteza gradnikov, biološko aktivnih majhnih molekul, fluorescenčnih označevalcev in prob
Raziskovalci na Katedri za farmacevtsko kemijo imamo številne izkušnje in znanje za razvoj novih sinteznih poti in organske sinteze majhnih molekul (sinteznih gradnikov, intermediatov in biološko aktivnih spojin), ki jih uvrščamo med heterocikle, peptide, peptidomimetike, glikomimetike, steroidomimetike, lipidomimetike, naravne spojine in njihove analoge. Pri tem uporabljamo tako klasične kot tudi moderne metode organske sinteze (sinteza z mikrovalovi, ultrazvokom, paralelna sinteza in sinteza na trdnih nosilcih). Ukvarjamo se tudi s sintezo fluorescenčnih označevalcev za polimere, membrane in proteine ter prob, ki so občutljive na pH, redoks potencial ali polarnost okolja. Strukturo in čistoto ciljnih spojin zagotavljamo s uveljavljenimi metodami izolacije in čiščenja (tankoplastna in kolonska kromatografija, HPLC) v kombinaciji s karakterizacijo spojin s spektroskopskimi metodami (NMR, MS, IR, EPR, UV-VIS, fluorescenčna mikroskopija).
a) 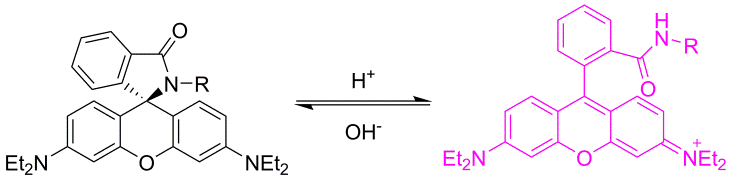 b)
b)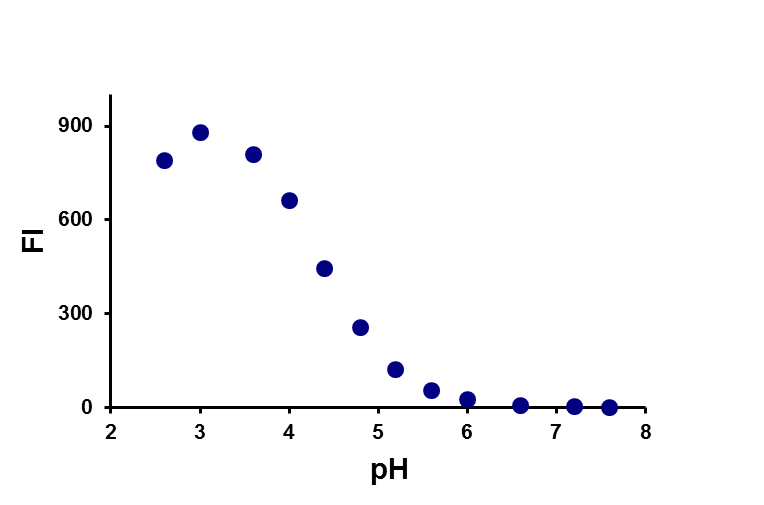
Primer od pH odvisne probe (a) in učinek pH na fluorescenco (b).
Zadnje objave in patenti:
1. Sova Matej, Frlan Rok, Gobec Stanislav, Stavber Gaj, Časar Zdenko. D-Glucosamine in iron-catalysed cross-coupling reactions of Grignards with allylic and vinylic bromides: application to the synthesis of a key sitagliptin precursor. Applied organometallic chemistry 2015, 29, 528-535, doi: 10.1002/aoc.3327.
2. Žula Aleš, Kikelj Danijel, Ilaš Janez. A convenient strategy for synthesizing the Agelas alkaloids clathrodin, oroidin, and hymenidin and their (un)saturated linker analogs. Tetrahedron Letters 2014, 55, 3999-4001, doi: 10.1016/j.tetlet.2014.05.087.
3. Mravljak Janez, Ojsteršek Tadej, Pajk Stane, Sollner Dolenc Marija. Coumarin-based dual fluorescent spin-probes. Tetrahedron Letters 2013, 54, 5236-5238, doi: 10.1016/j.tetlet.2013.07.084.
4. Mravljak Janez, Sova Matej, Kovač Andreja, Gobec Stanislav, Časar Zdenko. Process for the synthesis of ezetimibe and intermediates useful therefor: patent no. JP5735913 (B2) - 2015-06-17. Tokio: Japan Patent Office, 2015. 28 str.
5. Živec Matej, Gobec Stanislav, Anžič Borut, Zupet Rok, Kolenc Ivanka. Novel process for synthesis of pramipexole and its pharmaceutically acceptable salts : CN101622235 (B), 2012-07-25: applicant: Krka tovarna zdravil, d.d. Bejing: Chinese Patent Office, SIPO, 2012. 18 str.
6) Toksikologija pri odkrivanju zdravilnih učinkovin
Opis: Identifikacija metabolitov je pomemben vidik v različnih stopnjah razvoja zdravilnih učinkovin. Za določanje reaktivnih metabolitov uporabljamo kombinacijo in silico metode in in vitro testa »GSH trapping assay«, kjer nastale konjugate z glutationom v jetrnih mikrosomih in dodanim NADPH določamo z različnimi metodami LC-MS/MS spektroskopije. Razvijamo tudi in silico in in vitro metodo za ugotavljanje potenciala spojin kot endokrinih motilcev, ki lahko vplivajo tudi na imunski sistem. Endokrini motilci, kot je bisfenol A, lahko modulirajo endokrini sistem in ostale jedrne receptorje, tako da vplivajo na transport, vezavo in izločanje endogenih hormonov, ali pa je učinek epigenetski. V raziskavah bomo poskušali ugotoviti molekulske mehanizme teh učinkov in ovrednotiti ali zmesi endokrinih motilcev interagirajo med seboj in imajo sinergistični učinek.
Zadnje objave:
1. Gramec Darja, Schmidt Jan, Fic Anja, Klopčič Ivana, Trontelj Jurij, Sollner Dolenc Marija, Finel Moshe, Peterlin Mašič Lucija. Influence of metabolism on endocrine activities of bisphenol S. Chemosphere 2016, 157, 152-159, doi: 10.1016/j.chemosphere.2016.05.027.
2. Klopčič Ivana, Gramec Darja, Peterlin Mašič Lucija, Sollner Dolenc Marija. Comparison of in vitro hormone activities of novel flame retardants TBB, TBPH and their metabolites TBBA and TBMEPH using reporter gene assays. Chemosphere 2016, 160, 244-251, doi: 10.1016/j.chemosphere.2016.06.091.
3. Tišler Tatjana, Krel Alja, Gerželj Urška, Erjavec Boštjan, Sollner Dolenc Marija, Pintar Albin. Hazard identification and risk characterization of bisphenols A, F and AF to aquatic organisms. Environmental pollution 2016, 212, 472-479, doi: 10.1016/j.envpol.2016.02.045.
4. Gramec Darja, Tomašič Tihomir, Carino Adriana, Distrutti Eleonora, Fiorucci Stefano, Peterlin Mašič Lucija. New brominated flame retardants and their metabolites as activators of the pregnane X receptor. Toxicology Letters 2016, 259, 116-123, doi: 10.1016/j.toxlet.2016.08.005.
5. Fic Anja, Jurković Mlakar Simona, Juvan Peter, Mlakar Vid, Marc Janja, Sollner Dolenc Marija, Broberk Karin, Peterlin Mašič Lucija. Genome-wide gene expression profiling of low-dose, long-term exposure of human osteosarcoma cells to bisphenol A and its analogs bisphenols AF and S. Toxicology in vitro 2015, 29, 1060-1069, doi: 10.1016/j.tiv.2015.03.014.